9 charakteristických znakov starnutia
Prehľad 9 základných znakov starnutia
Starnutie je charakterizované progresívnou stratou fyziologickej integrity, ktorá vedie k zhoršenej funkcii tela a zvýšenej šance na smrť. Starnutie je hlavným rizikovým faktorom pre mnoho ľudských ochorení vrátane rakoviny, cukrovky, kardiovaskulárnych porúch a neurodegeneratívnych chorôb. Výskum starnutia zaznamenal v posledných rokoch bezprecedentný pokrok, najmä vďaka zisteniu, že rýchlosť starnutia je kontrolovaná, aspoň do určitej miery, genetickými cestami a biochemickými procesmi zachovanými v evolúcii. Tento článok opisuje 9 charakteristických znakov, ktoré predstavujú spoločné menovatele starnutia ľudského tela.

1. Epigenetická dysregulácia
Epigenetická dysregulácia môže byť jedným z najdôležitejších dôvodov, prečo starneme. Epigenóm určuje, ktoré gény sú aktívne a ktoré nie. Na epigenóm sa môžeme pozerať ako na vypínač alebo zapínač našich génov. Keď starneme, epigenóm sa stáva dysregulatívnym. Gény, ktoré by sa mali vypnúť, sa zapnú (ako napríklad gény podporujúce rakovinu) a gény, ktoré by mali ostať zapnuté sa vypnú (ako gény, ktoré chránia a opravujú naše bunky). Taktiež sa nesmierne zložité mechanizmy, ktoré likvidujú našu DNA, stanú menej organizovanými, takže DNA a nakoniec celá bunka sa stane nestabilnou.
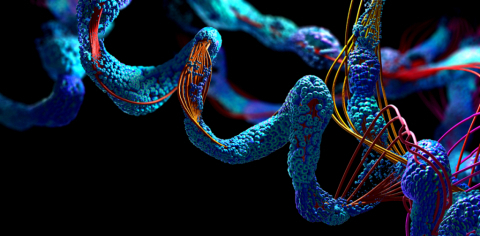
2. Akumulácia bielkovín
Bielkoviny (proteíny) sú stavebnými kameňmi našich buniek. Bunka obsahuje milióny bielkovín, ktoré sa kontinuálne hromadia a rozkladajú v komplexnom a zložitom recyklačnom procese. Tento proces však nie je dokonalý. Sem-tam sa bielkoviny nerozložia a začnú sa zdržiavať a hromadiť v bunkách a okolo nich a bránia tak správnemu fungovaniu buniek. Táto „bielkovinová toxicita“ spôsobená tzv. stratou proteostázy (bielkovinová homeostáza) je jedným z dôvodov, prečo starneme.
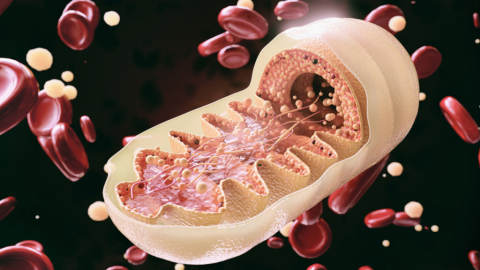
3. Mitochondriálna dysfunkcia
Mitochondrie sú elektrárne našej bunky. Každá bunka môže obsahovať stovky až tisíce mitochondrií. Mitochondrie produkujú energiu, ktorú potrebujeme pre život. V skutočnosti kyslík, ktorý dýchame a jedlo, ktoré jeme, pretvárajú mitochondrie na energiu, ktorú používame na pohyb, premýšľanie a prežitie. Čím sme starší, tým viac sa mitochondrie poškodzujú. Bez dostatočne fungujúcich mitochondrií, bunky prestávajú fungovať efektívne alebo sa začnú rozpadať, čo vedie k príznakom starnutia.

4. Skracovanie telomér a ich poškodenie
Teloméry sú vonkajšími koncami nášho vlákna DNA. Teloméry sú zložené z opakujúcej sa DNA a chránia jej konce. Rovnako ako plastové hlavičky na koncoch našich šnúrok, ktoré ich chránia pred rozmotaním. S každým delením buniek sa teloméry skracujú, až kým nie sú také krátke, že nedokážu dostatočne chrániť DNA. V nedeliacich sa bunkách (v ktorých sa teloméry neskracujú) to nie je problém. Napriek tomu sa môžu tieto bunky poškodiť, pretože deliace sa okolité bunky, ktoré vyživujú a chránia nedeliace bunky, sú poškodené kvôli skráteniu svojich telomér. Počas starnutia sa teloméry nielen skrátia, ale aj poškodia, čo vytvára ďalší stres pre naše bunky.

5. Akumulácia senescentných buniek
Ako starneme, všade v našich tkanivách sa začína objavovať čoraz viac senescentných buniek. Senescentné bunky boli v skutočnosti zdravými bunkami, ktoré však za svoj život nahromadili mnoho poškodení. Za normálnych okolností by mali tieto bunky odumrieť, avšak senescentné bunky ostávajú v okolí zdravých buniek a vylučujú látky, ktoré ich poškodzujú. Akumulácia senescentných buniek v pokožke prispieva napríklad k vráskam. Starnúce bunky v cievach spôsobujú, že cievy sú tuhšie a náchylnejšie na aterosklerózu. Starnúce bunky v mozgu prispievajú k jeho zápalu a starnutiu.

6. Nestabilita genómu (DNA)
Zdá sa, že pri nestabilite genómu zohrávajú úlohu zlomy dvojvláknovej DNA alebo iné formy jej poškodenia. Niektorí vedci však predpokladajú, že poškodenie DNA môže urýchliť starnutie nepriamo. Na opravu zlomov DNA sa špecifické opravné enzýmy odlákajú od svojho obvyklého miesta pôsobenia, kde obvykle pomáhajú stabilizovať epigenóm. Keď dôjde k mnohým zlomom DNA, enzýmy nemôžu správne udržiavať epigenóm, pretože musia opraviť praskliny DNA, čo môže viesť k dysregulovanému epigenómu, dôležitému faktoru starnutia. Počas starnutia tiež začnú skákať špecifické časti našej DNA a náhodne sa vkladať do iných oblastí DNA čo tiež prispieva k nestabilite genómu.
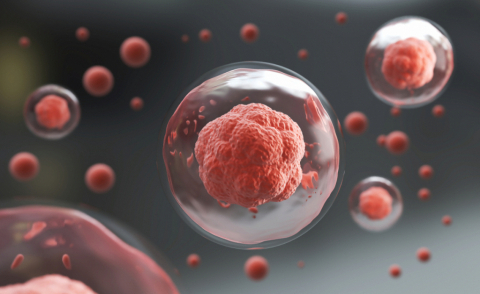
7. Úbytok kmeňových buniek
Kmeňové bunky tvoria nové bunky, ktoré dopĺňajú naše tkanivá. Napríklad neuronálne kmeňové bunky vytvárajú neuróny. Hematopoetické kmeňové bunky produkujú červené a biele krvinky. Počas starnutia klesá množstvo kmeňových buniek v tele. Zvyšné kmeňové bunky navyše fungujú horšie. To vedie k tomu, že naše tkanivá sú menej udržiavané, opravované a doplňované novými bunkami, čo prispieva k starnutiu.
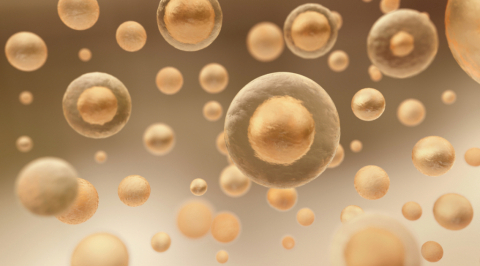
8. Pozmenená medzibunková komunikácia
Bunky, ktoré tvoria naše telo sa nesprávajú navzájom izolovane. Bunky sú neustále vystavené obrovskému a rôznorodému spektru vonkajších signálov, z ktorých niektoré pochádzajú zo susedných buniek, iné sú prenášané krvou zo vzdialených tkanív alebo majú formu elektrických signálov. Bunky nášho tela môžu byť ovplyvnené aj signálmi pochádzajúcimi z baktérií v našich črevách. Keď starneme, komunikácia medzi bunkami sa mení. Napríklad senescentné bunky, vylučujú látky, ktoré poškodzujú ďalšie zdravé bunky. Tieto starnúce bunky tiež vylučujú prozápalové látky, ktoré sa dostávajú do celého tela a spôsobujú tak zápal a iné škody v celom organizme.

9. Deregulovaná citlivosť na živiny
Bunky v našom tele vyžadujú neustály prísun živín. Energiu z nich bunky potrebujú na svoje fungovanie, avšak náš príjem živín nie je pravidelný. Bunky preto musia byť schopné uchovávať živiny, keď ich je dostatok, a mať prístup k týmto zásobám, keď je živín nedostatok. Počas starnutia bunky strácajú citlivosť napríklad voči inzulínu, ktorý signalizuje našim bunkám aby absorbovali cukor z nášho krvného obehu, čo vedie k inzulínovej rezistencii, predštádiu cukrovky. Ďalšími ovplyvnenými sú najmä mTOR, zodpovedný za monitorovanie vysokých koncentrácií aminokyselín. AMPK, ktorý sníma stavy nízkej energie detekciou vysokých hladín AMP a sirtuíny, ktoré detegujú vysoké hladiny NAD + a monitorujú stavy nízkej energie. 1, 2
Čítajte ďalej: Potenciálne doplnky dlhovekosti
Použitá literatúra
1. https://www.ncbi.nlm.nih.gov/…/PMC3836174/
2. https://www.cell.com/…13%2900645-4
